[MIM 161 800, 256 030, 605 355]
(Nemaline rod myopathy, myopathies némalines)
Rare : 1/50.000 sauf la forme des Amish où la prévalence est de 1/500. . En général sporadique (65%) mais des formes de transmission autosomique récessive et dominante existent. Dix gènes sont associés à cette myopathie sans corrélation précise entre le génotype et la sévérité du phénotype:
|
acronyme |
gĶne |
locus |
|
protķine |
MIM |
clinique |
|
NEM1 |
TPM3 |
1q21.3 |
AD |
tropomyosine 3 |
609 284 |
|
|
NEM2 |
NEB |
2q23.3 |
AR |
nķbuline |
256 030 |
|
|
NEM3 |
ACTA1 |
1q42.13 |
AD |
actine ß1 muscles |
161 800 |
50 % formes nķonatales sķvĶres |
|
NEM4 |
TPM2 |
9p13.3 |
AD |
tropomyosine 2 |
609 285 |
|
|
NEM5 |
TNNT1 |
19q13.42 |
AR |
troponine T type 1 |
605 555 |
surtout population Amish |
|
NEM6 |
KBDT13 |
15q22.31 |
AD |
Kelch repeat abd BTP domain |
609 273 |
|
|
NEM7 |
CFL2 |
14q13.1 |
AR |
cofiline |
601 443 |
|
|
NEM8 |
KLH40 |
3p22.1 |
AR |
Kelch-like family member 40 |
615 348 |
|
|
NEM9 |
KLH41 |
2q31.1 |
AR |
Kelch-like family member 41 |
615 731 |
|
|
NEM10 |
LMOD3 |
3p14.1 |
AR |
lķiomodine 3 |
616 165 |
|
|
NEM11 |
MYPN |
10q21.3 |
AR |
myopalladine |
617 336 |
|
Dans certains cas, une mutation des gènes RYR1 (19q13.2) ou NEB ou KBTBD3 entraîne l’apparition de « core » centraux et on parle de core-rod myopathy (voir central core disease).
Une mutation du gène ACTA1 peut également entraîner une myopathie à corps zébrés qui est considérée comme une variante de la myopathie à bâtonnets. Une autre variante est la cap myopathy où l’on observe un réarrangement des filaments fins : elle se présente comme une forme typique de myopathie à bâtonnets mais l’image histologique montre une « coiffe » en périphériue des fibres musculaires. Elle est associée à des mutations des gènes ACTA1, TPM3 ou TPM2.
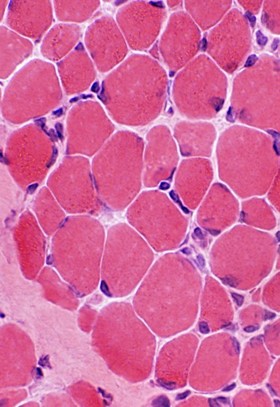
Les bâtonnets visibles en microscopie optique ou électronique correspondent à des inclusions cytoplasmiques dérivées des protéines (actine, α-actinine) de la zone Z des fibres musculaires.
Au moins 4 tableaux cliniques ont été décrits :
- forme congénitale sévère (ACTA-1, NEB, KLHL 40, LMOD3) : atteinte musculaire massive avec absence de motricité spontanée nécessitant une ventilation assistée et une alimentation par gavage ; le décès survient habituellement dans la 1ère année de vie.
- forme congénitale intermédiaire (NEB) (il existe aussi une forme connue sous le nom de Amish nemaline myopathy: TNNT1): hypotonie et faiblesse musculaire généralisée qui apparaissent à quelques mois de vie ; retard important de développement : ni marche ni station assises ne sont acquises ; scoliose et contractures musculaires avec insuffisance respiratoire précoce.
- forme typique (NEB, TPM2): début à un âge variable, atteinte musculaire diffuse avec amyotrophie et rétractions musculaires marquées, syndrome restrictif, troubles de déglutition et un faciès étroit avec pro- ou micrognathie, qui peut entraîner des difficultés d'intubation.
- forme débutant dans l’enfance ou l’adolescence (TPM3) : apparition tardive d’une faiblesse musculaire en général proximale
On peut également observer :
- une forme débutant à l'âge adulte : sporadique ; se généralise rapidement avec décès par atteinte cardiaque ; environ 50% de ces formes à début tardif sont acquises et associées à une gammapathie monoclonale bénigne à IgG (MGUS acronyme de monoclonal gammapathy of undetermined significance) et répondent en partie à la corticothérapie associée ou non à l’azathioprine, voire à une greffe de moelle.
- une forme asymptomatique : rare, uniquement décelée lors d'une biopsie musculaire de dépistage familial.
- une atteinte cardiaque surtout dans les cas liés à une mutation du gène ACTA1 : cardiomyopathie dilatée, insuffisance cardiaque, troubles du rythme ventriculaire.
Les CPK sont peu ou pas élevés. Décès par insuffisance respiratoire progressive souvent aggravée par des pneumonies d’inhalation secondaires à une atteinte bulbaire.
Dans certains cas, une mutation des gĶnes RYR1 (19q13.2) ou NEB ou KBTBD3 entraŅne l’apparition de ½ĀcoreĀ╗ centraux et on parle de core-rod myopathy (voir central core disease).
Une mutation du gĶne ACTA1 peut ķgalement entraŅner une myopathie Ó corps zķbrķs qui est considķrķe comme une variante de la myopathie Ó bŌtonnets.
Une autre variante est la cap myopathy (voir ce terme) o∙ l’on observe un rķarrangement des filaments finsĀ: elle se prķsente comme une forme typique de myopathie Ó bŌtonnets mais l’image histologique montre une ½ĀcoiffeĀ╗ en pķriphķrie des fibres musculaires. Elle est associķe Ó des mutations des gĶnes ACTA1, TPM3 ou TPM2.
Une mutation du gĶne MYO18B (22q12.1) [MIM 616 549] entraŅne l’association d’une myopathie Ó bŌtonnets, d’une dysmorphie faciale et d’un syndrome de Klippel-Feil (voir ce terme).
La myopathie dite Ó nemaline bodies [MIM 620 310] est trĶs rare et due est la transmission autosomique rķcessive d’une mutation du gĶne RYR3 (15q13-Q14). La biopsie musculaire montre une grande variation de taille des fibres musculaires avec une prķdominance des fibres de type 1 et une atrophie avec de nombreux ½Ācorps de nķmalineĀ╗ situķs autour du noyau, dans le cyoplasme dans sous le sarcolemme.
Dans la myopathie Ó bŌtonnets, les bŌtonnets visibles en microscopie optique ou ķlectronique correspondent Ó des inclusions cytoplasmiques dķrivķes des protķines (actine, α-actinine) de la zone Z des fibres musculaires.
Implications anesthésiques:
Y penser en cas de retard d’acquisition de la marche ou de fatigue musculaire rapide Ó l’exercice ou d’association de dysarthrie, contractures, scoliose. Echographie cardiaqueĀ: cardiomyopathieĀ? hypertension artķrielle pulmonaire secondaire Ó l’hypoxķmie chroniqueĀ? Le patient est parfois porteur d’un dķfibrillateur cardiaque interne automatique.
Aucun cas d’hyperthermie maligne associķ Ó la myopathie Ó bŌtonnets n’a ķtķ publiķ. Cependant, en cas de mutation RYR1 ou de ½ĀcoreĀ╗ centraux, il y a un risque d’hyperthermie maligneĀ: cette prķcaution est par prudence ķtendue Ó tous les patients souffrant de cette forme gķnķtique de la myopathie et dont le gķnotype prķcis n’est pas connu. Eviter la succinylcholine comme pour toutes les myopathies mais les agents halogķnķs ont ķtķ utilisķs sans provoquer de rhabdomyolyse. Risque d’intubation difficileĀ: atteinte prķcoce des muscles du visage et du cou. Ventilation nocturne en cas d’insuffisance respiratoire sķvĶre. Amyotrophie et troubles de dķglutition.
Références :
- Shenkman Z, Sheffer O, Erez I, Litmanovic I, Jedeikin R. Spinal anesthesia for gastrostomy in an infant with nemaline myopathy. Anesth Analg 2000; 91: 858-9.
- Heard SO, Kaplan RF. Neuromuscular blockade in a patient with nemaline myopathy. Anesthesiology 1983; 59: 588-90.
- Klingler W, Rueffert H, Lehmann-Horn F, Girard T, Hopkins PM. Core myopathies and risk of malignant hyperthermia. Anesth Analg 2009; 109: 1167-73.
- Deconinck N, Laterre EC, Van den bergh PYK.
Adult-onset nemaline myopathy and monoclonal gammapathy: a case report.
Acta Neurol Belg 2000; 100: 34-40. - Ryan MM, Schnell C, Trsickland CD, Shield LK et al.
Nemaline myopathy: a clinical study of 143 cases.
Ann Neurol 2001; 50: 312-20. - Desaegher J, Vanmarsenille J-M, Vekemans M-C, Van den Bergh PYK.
Myopathie némaline sporadique à début tardif avec gammapathie monnoclonale : traitement par cellules souches hématopoïétiques.
Louvain med 2014 ; 133 : 522-6. - Raveau T, Lassalle V, Dubourg O, Legout A, Tirot P.
Révélation d’une myopathie à bâtonnets de l’adulte par une insuffisance respiratoire aiguë après chirurgie ambulatoire de la cataracte.
Ann Fr Anesth Réanim 2012 ; 31 : 638-40. - Brislin RP, Theroux MC.
Core myopathies and malignant hyperthermia susceptibility : a review.
Pediatr Anesth 2013 ; 23 : 834-41. - Christiaens F, Van den Bergh PYK.
Les myopathies congénitales.
Louvain Med 2014 ; 133 : 478-90. - North K, Wang C, Clarke N, Jungbluth H, Vainzof M, Dowling J et al.
Approach to the diagnosis of congenital myopathies.
Neuromuscul Disord 2014 ; 24 : 97-116. - Tran NH, Chhibber A.
Anesthetic management of a pediatric patient with NEB1-genotype nemaline rod myopathy for cleft palate repair.
Pediatr Anesth Crit Care J 2016; 4: 78-82 - Tran NH, Smith D.
Anesthetic consideration for patients with nemaline rod myopathy: a literature review.
Pediatr Anesth Crit Care J 2017; 5: 31-9. - Oliveira M, Fernandes AL.
Using sevoflurane in a pediatric patient with nemaline rod myopathy.
Pediatr Anesth 2018; 18: 749-50 - Benarroch L, Bonne G, Rivier F, Hamroun D.
The 2020 version of the gene table of neuromuscular disorders. Neuromusc Dis 2019Ā; 29Ā: 980-1018 ou http://www.musclegenetable.fr - Jung H, Kim H, Lee SW.
Anesthetic management for surgery in a nemaline myopathy patient with difficult airway: a CARE-compliant case report.
Medicine 2023;102:46(e36174). doi.org/10.1097/MD.0000000000036174
Mise à jour juillet 2024