(hķpatoblastome, hķpatocarcinome, sarcome embryonnaire indiffķrenciķ, hamartome, Hķmangioendothķliome , Hyperplasie focale nodulaire, adķnome)
- Hķpatoblastome [MIM 114 550]
Reprķsente 1 Ó 2% des tumeurs malignes de l’enfant. Mutation somatique du gĶne APC (5q22.2). Tumeur d’origine embryonnaire qui atteint principalement l’enfant de moins de 2 ans. Elle est souvent associķe Ó une malformation somatique commeĀ:
- un syndrome de Beckwitt-Wiedemann
- une hķmihypertrophie corporelle.
Les facteurs de risque sont une naissance prķmaturķe (<1500 g), une polypose rectocolique familiale, un tabagisme durant la grossesse et une prķķclampsie. Mais aussiĀ: le syndrome de Li Fraumeni (voir ce terme) ou la trisomie 18.
Les signes sont en gķnķral une masse abdominale peu symptomatique dķcouverte par hasard. La douleur et l’ictĶre sont rares. La prķsentation sous forme d’hķmorragie intra-tumorale ou de rupture intra-pķritonķale (Ó l’occasion d’un traumatisme) est exceptionnelle.
Une augmentation massive du taux sķrique d’α-f£toprotķine est observķe dans 75% des cas. Il peut exister des mķtastases pulmonaires. Deux syndromes paranķoplasiques sont parfois observķsĀ:
- une thrombocytose, par sķcrķtion de thrombopo’ķtine ;
- une pseudopubertķ prķcoce, par sķcrķtion de Ō-HCG.
Selon l’histologie, on distingueĀ:
- les formes purement ķpithķliales (la majoritķ des cas)
- les formes mixtes ķpithķliales et mķsenchymateuses et, en fonction du contingent ķpithķlial, quatre types histologiques sont individualisķs : f£tal, embryonnaire, Ó petites cellules indiffķrenciķes et macrotrabķculaire.
Le traitement consiste en plusieurs cures de chimiothķrapie (cisplatine, doxorubicine) suivies de la rķsection chirurgicale ou d’une transplantation hķpatique si la tumeur n’est pas rķsķcable (PRE-TEXT IV).
- HķpatocarcinomeĀ: [MIM 114 550]
Tumeur rare chez l’enfant. Sa frķquence augmente avec l’Ōge. Mutation somatique du gĶne CASP8 (2p33.1), CTNNB1 (3p22.1), PIK3CA (3q26.32, MET (7q31.2), PDGFRL (8p22), AXIN1 (16p13.3) ou TP53 (17p13.1). Elle survient parfois sur un terrain cirrhotiqueĀ: hķpatite B ou C, tyrosinķmie I, glycogķnose Ia (voir ces termes).
Les signes consistent en gķnķral en une masse abdominale douloureuse avec altķration de l’ķtat gķnķral. L’augmentation du taux sķrique d’α-f£toprotķine est moins importante et moins frķquente qu’en cas d’hķpatoblastome. Deux syndromes paranķoplasiques peuvent Ļtre observķsĀ:
- une polycythķmie ;
- une fķminisation chez le garńon.
Le pronostic est moins bon que celui de l’hķpatoblastome et la chimiothķrapie est moins efficace. Le traitement consiste en une rķsection chirurgicale ou une transplantation hķpatique si la tumeur n’est pas rķsķcable.
- Hķpatocarcinome fibrolamellaire
RarissimeĀ: reprķsente 1 Ó 9% des tumeurs hķpatiques. Variante histologique de l’hķpatocarcinome, d’ķvolution trĶs lente et qui se dķveloppe sur un foie sain. Les cellelues tumorales expriment en quantitķs importantes la protķine chimķrique DNAJB1-PRKACA suite Ó une dķlķtion au niveau du chromosome 19. Les taux sanguins de transcobalamine I et ou II sont ķlevķs, ce qui permet de suivre l’ķvolution de la tumeur.
Tumeur rare de l’enfant de 6 Ó 10 ans. Il s’agit d’une masse abdominale d’allure kystique. Le pronostic est sķvĶreĀ: mķtastases pulmonaires, pleurales, pķritonķales frķquentes.
- Tumeur rhabdo’de du foie [MIM 609Ā322, 613Ā325]
TrĶs rare. En gķnķral chez le nourrisson ou le petit enfant. Tumeur sarcomateuse trĶs agressive. Mutation germinale (transmission autosomique dominante d’une prķdisposition familiale aux tumeurs rhabdo’des) ou somatique du gĶne SMARCB1 (22q11.23).
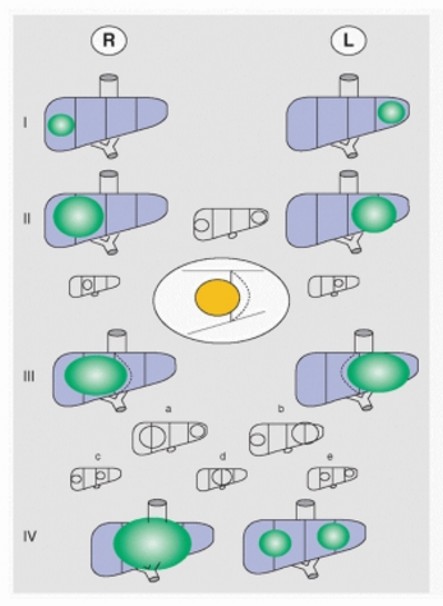
Pour toutes ces trois types de tumeurs malignes du foie, la mise au point radiologique permet un bilan d’extension prķ-et post-chimiothķrapieĀen fonction du nombre de secteurs hķpatiques envahis, de l’envahissement des vaisseaux, d’une extension extrahķpatique et de la prķsence de mķtastasesĀ: bilan PRET-EXT et POST-TEXT (SIOPEL)
- stade I : la tumeur ne touche qu’un seul secteur hķpatique
- stade II : la tumeur touche deux secteurs hķpatiques adjacents
- stade III : la tumeur touche trois secteurs hķpatiques adjacents ou deux
- stade IV : la tumeur touche les quatre secteurs hķpatiques
Les ķlķments suivants permettent d'affiner la stadification :
- E = une extension extra-hķpatique de la tumeur 1, 2
- F = tumeur multifocale
- M = mķtastasesĀ: 1 si mķtastases Ó distance.
- V = atteinte des 3 veines sus-hķpatiquesĀ: 1, 2, 3
- P = atteinte du tronc porte ou de ses 2 branchesĀ: 1, 2
- C1 = atteinte du lobe caudķ (segment 1)
- R = rupture tumorale au moment du diagnostic
- N = atteinte ganglionnaire
Traitements possiblesĀ: cures de chimiothķrapie suivies d’une hķpatectomie plus ou moins ķtendue, chimioembolisation de la tumeur, embolisation prķopķratoire, transplantation hķpatique.
- Hamartome mķsenchymateux (Maladie des complexes de von Meyenburg)
Reprķsente environ 8% des tumeurs hķpatiques de l’enfant. Tumeur bķnigne solide qui apparaŅt gķnķralement avant l’Ōge de 2 ans. Elle est associķe Ó une mutation du gĶne MALAT1(11q13), C19MC (19q13.4) ou, plus rarement, d’une mutation germinale ou somatique du gĶne DICER1 (14q32.13) (voir ce terme). Elle est soit appendue Ó un lobe hķpatique (photo) soit bien encapsulķe dans le foie.
En cas de multiples micro-hamartomes biliaires localisķs dans les rķgions sous-capsulaires, on parle de maladie des complexes de von MeyenburgĀ: ces lķsions sont bķnignes et se composent de petits canaux biliaires au sein d’un stroma fibreux frķquemment hyalinisķ. Ils sont souvent asymptomatiques et ne nķcessitent aucun traitement.

- Hķmangio-endothķliome
Tumeur vasculaire qui apparaŅt durant les 6 premiers mois de vie puis prķsente une phase de croissance de 6 Ó 8 mois avant de se stabiliser puis d’entamer une rķgression spontanķe lente Ó partir de l’Ōge de 18 mois-2 ans jusque vers 6-8 ans. C’est une lķsion multifocale souvent accompagnķe de lķsions cutanķes qui se prķsente sous la forme d’une hķpatomķgalie mais qui entraŅner une dķcompensation cardiaque. └ l’heure actuelle, le propranolol (associķ ou on Ó la corticothķrapie) est utilisķ avec succĶs Ó la dose de 2 Ó 3,5 mg/kg/jour. On ķvite si possible la chirurgie (en gķnķral, la transplantation hķpatique) qui est trĶs hķmorragique et grevķe d’une mortalitķ et d’une morbiditķ importantes.
- Adķnome
Tumeur bķnigne, en gķnķral unique mais qui peut Ļtre multiple (½Āadķnomatose hķpatocellulaireĀ╗) qui est une complication tardive de la glycogķnose Ia (une transformation maligne est possible en cas de mutation somatique du gĶne IGF2R (6q25.3)) III (maladie de Cori) ou IV, et de la Ō-thalassķmie. Facteurs favorisantsĀ: diabĶte MODY 3, fistule portosystķmique congķnitale, utilisation d’androgĶnes anabolisants ou de contraceptifs oraux, polypose adķnomateuse familiale, syndrome de Klinefelter.
TraitementĀ: surveillance, risque de transformation maligne (10%).
- Hyperplasie focale nodulaire
Tumeur bķnigne non ķvolutive, plus frķquente chez l’adolescente. Elle serait peut-Ļtre la consķquence d'uneĀhypervascularisation localisķe du foie. Chez la femme adulte, elle serait favorisķe par la contraception orale.
Implications anesthésiques:
- en cas de chimiothķrapies prķopķratoiresĀ: contr¶le de l’hķmogramme et de l’hķmostase mais aussi ECG et ķchocardiographie pour vķrifier la fonction myocardique.
- voir les examens prķopķratoires (ķchographie, CT-scan, parfois cavographie) nķcessaires pour connaŅtre l’anatomie prķcise, la vascularisation de la tumeur et ses rapports avec les gros vaisseaux, Ó la recherche d'une compression ou d'un envahissement de la veine cave infķrieure (VCI).
- inductionĀ inhalatoireĀou intraveineuseĀ; utiliser une sonde endotrachķale Ó ballonnet pour ķviter des problĶmes ventilatoires lors de la pose des ķcarteursĀabdominaux. L’entretien est assurķe par une ventilation contr¶lķe avec une PEP Ó l’aide d’un mķlange O2/air associķ Ó l’isoflurane ou au sķvoflurane et un morphinique (fentanyl, sufentanil, en bolus rķpķtķs ou en perfusion continue).
- la fonction hķpatique est habituellement normale (sauf en cas de cirrhose prķexistante) et s’il n’y a pas de troubles de coagulation, l’association d’une anesthķsie gķnķrale et d’une pķridurale thoracique basse donne d’excellents rķsultats. Il faut cependant garder Ó l’esprit qu’en cas d’hķpatectomie ķtendue une insuffisance hķpatique plus ou moins importante, avec troubles modķrķs de l’hķmostase et diminution des capacitķs mķtaboliques du foie, est inķvitable durant les premiers jours postopķratoires. Le rapport risque/bķnķfice de la technique doit donc Ļtre ķvaluķ de maniĶre individualisķe
- monitorage invasif pour ķvaluer et compenser les pertes et les consķquences mķtaboliques d’une hķpatectomie : mesure invasive de la pression artķrielle, cathķter veineux central, sonde urinaire. Il est prķfķrable de placer les voies veineuses aux membres supķrieurs pour pouvoir continuer Ó assurer un remplissage vasculaire efficace en cas de clampage de la VCI. En cas d’extension intravasculaire tumorale de la VCI ou de l’oreillette droite (OD), l’intervention chirurgicale est gķnķralement rķalisķe sous circulation extra-corporelle (CEC).
- pour faciliter la dissection chirurgicale, il est important d’ķviter un remplissage vasculaire trop important car cela augmente la turgescence du rķseau porte et de la VCI et donc le risque de saignement. Le remplissage est guidķ par la valeur de pression artķrielle systolique PAs et les variations de son pic avec la ventilation contr¶lķe mais aussi par l’observation du champ opķratoireĀcar certaines modifications sont dues aux manoeuvres chirurgicalesĀ: mobilisation du foie ou compression d’un gros vaisseau..
- en cas de clampage des vaisseaux du hile hķpatique ou d’exclusion vasculaire du foie (clampage des vaisseaux du hile et de la veine cave infķrieure supra- et intra-hķpatique), le chirurgien doit d’abord procķder Ó un essai de clampage pour en observer les consķquences hķmodynamiques et permettre d’adapter le remplissage de l’enfant avant le clampage dķfinitif. Le clampage du hile est habituellement bien tolķrķ si l’enfant n’est pas hypovolķmique mais l’exclusion vasculaire requiert parfois l’administration de noradrķnaline. Si un clampage prolongķ est prķvu, il est prķfķrable de l’interrompre toutes les 15-20 minutes pour diminuer les sķquelles ischķmiques au niveau hķpatocytaire.
- un risque d’embolie gazeuse ou tumorale est prķsent durant toute l’intervention, particuliĶrement durant la dissection et au moment du dķclampage des vaisseaux hķpatiques.
- cas particulierĀ: la rķsection ex-situ de la tumeur (rare)Ā: le foie est retirķ en entier du patient (hķpatectomie totale) et dissķquķ dans un liquide de conservation glacķ pour pouvoir en ¶ter la masse tumorale. ╔tant donnķ l’absence d’hypertension portale, il faut alors prķvoir une circulation extracorporelle partielle veino-veineuse pour maintenir le dķbit cardiaque durant cette phase d’anhķpatie. On peut par exemple utiliser un introducteur de Swan Ganz 8 Fr placķ dans une veine jugulaire interne : le bras latķral peut en Ļtre connectķ stķrilement au circuit de CEC hķparinisķ aprĶs cannulation des veines fķmorale et porte, pour assurer le retour veineux splanchnique et des membres infķrieurs au c£ur.
Un ictĶre et/ou de l’ascite peuvent se constituer durant les 2 Ó 5 premiers jours postopķratoires.
D’autres complications hķpatiques sont possibles:
- une hķmorragie/ hķmatome sur la tranche de sectionĀ;
- une fistule biliaire sur la tranche de sectionĀ: en l’absence d’extķriorisation par un drain, le premier signe clinique est la douleur (irritation pķritonķale par la bile) ; il faut ķgalement suspecter le diagnostic en cas d’ķlķvation de la bilirubine plasmatique car l’ķcoulement de bile dans le pķritoine est rķsorbķĀ;
- une dķcompensation hķpatocytaire : Ó suspecter en cas d’hķpatectomie ķtendue et/ou d’exclusion vasculaire totale du foie. La dķcompensation hķpatique est signalķe par une poussķe ascitique, un ictĶre, des troubles de la conscience (encķphalopathie) et de la coagulation (INR et taux de facteur V bas).
Références :
- Mazereeuw-Hautier J, Hoeger PH, Benlarech S, Ammmour A, Broue P et al
Efficacy of propranolol in hepatic infantile hemangiomas with diffuse neonatal hemangiomatosis.
J Pediatr 2010Ā; 157:340-2.
- Markiewicz-Kijewska M, Kasprzyk W, Broniszczak D, Bacewicz L, Ostoja-Chyzynska A, Ismael H, Kosciesza A et al
Hemodynamic failure as an indication to urgent liver transplantation in infants with giant hepatic hemangiomas or vascular malformations: report of four cases.
Pediatr Transplant 2009; 13:906-12.
- Przybylo HJ, Stevenson GW, Backer C, Luck SR, Webb CL, Morgan E, Hall SC.
Anesthetic management of children with intracardiac extension of abdominal tumors.
Anesth Analg 1994; 78:172-5.
- Lentschener C, Ozier Y.
Anaesthesia for elective liver resectionĀ: some points should be revisited.
Eur J Anaesthesiol 2002; 19:780-8.
- Dorman F, Sumner E, Spitz L.
Fatal intraoperative tumor embolism in a child with hepatoblastoma.
Anesthesiology 1985; 63:692-3.
Mise-à-jour juillet 2020