Affection fréquente. Dans 35% des cas, un membre de la fratrie est atteint, ce qui justifie une exploration systématique de la fratrie d’un enfant atteint. Le reflux vésico-urétéral prédispose aux infections urinaires et, en particulier ŕ la pyélonéphrite, sa forme la plus grave. Ces infections récurrentes sont souvent un mode révélateur de la maladie et menacent la fonction rénale. La réalisation d’une échographie mictionnelle en cas d’infection urinaire chez l’enfant permet de faire le diagnostic sans exposer l’enfant ŕ une irradiation importante.
On distingue :
- Reflux primitif
Anomalie congénitale de la jonction urétéro-vésicale qui associe ŕ des degrés divers 3 éléments : une laxité du trigone, une déficience des fibres musculaires de l’uretčre terminal et un trajet sous muqueux trop court avec ectopie latérale du méat.
- Reflux secondaire ŕ une lésion anatomique suite ŕ
- destruction chirurgicale du mécanisme valvulaire.
- sclérose du détrusor.
- vessie neurologique.
- anomalie congénitale de l’implantation urétéro-vésicale (uretčre ectopique ou surnuméraire).
- obstacle cervico-urétral.
- Reflux secondaire ŕ l’infection urinaire aiguë
Il y a probablement des jonctions ŕ la limite de la compétence pour lesquelles, l’infection urinaire (notamment ŕ bacilles Gram -) entraîne une béance du méat et favorise un RVU.
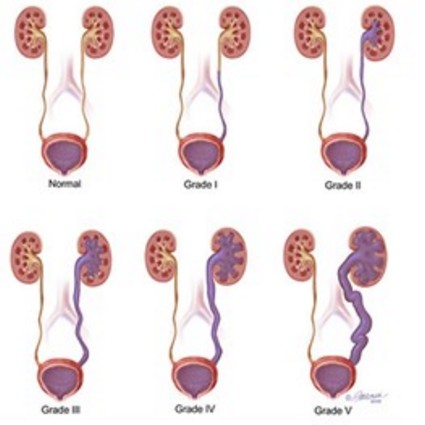
La classification internationale de Duckett comporte cinq stades :
Type I : reflux dans un uretčre pelvien fin.
Type II : reflux total sans dilatation urétéro-pyélo-calicielle.
Type III : dilatation urétéro-pyélique modérée sans atteinte calicielle.
Type IV : dilatation urétéro-pyélo-calicielle avec bombement et déformation des papilles.
Type V : dilatation et tortuosité urétérale majeure, grosse dilatation pyélo-calicielle avec perte de la vision des papilles.
Il faut ajouter ŕ ces 5 stades la notion du reflux intra-rénal qui peut ętre présent dans les stades IV et V et apparaît comme un facteur de gravité.
Le traitement du reflux vésico-urétral est controversé car la prise en charge actuelle, a dominante médicale est associée ŕ un fort taux de survenue d’une hypertension artérielle ŕ l’âge adulte. Le traitement initial est médical et consiste en une antibiothérapie, curative d'abord, puis prophylactique quotidienne, tant que l'enfant n'a pas acquis de contrôle sphinctérien, de maničre ŕ maintenir la stérilité des urines. Une surveillance échographique réguličre est assurée, tous les 3 ŕ 6 mois habituellement. Ultérieurement ou en cas de récidive infectieuse, on pratique une cystographie mictionnelle et/ou une étude isotopique pour déterminer le grade du reflux, son évolution et son retentissement sur la fonction rénale.
Il existe 3 types de procédures chirurgicales dont le but est de rétablir un environnement musculaire suffisant autour de la portion terminale de l'uretčre et créer ou prolonger son trajet sous-muqueux (au moins 5 fois le diamčtre de l'uretčre) de maničre ŕ éviter le reflux d'urine vésicale dans l'uretčre au moment de la miction:
- l'injection par voie endoscopique de macroplastique ou d'un autre polymčre synthétique autour de l'abouchement des uretčres dans la vessie: il s'agit d'un geste simple, rapide et peu invasif mais dont le taux de succčs ŕ long terme est limité ;
- l'abord extravésical des uretčres;
- l'abord intravésical des uretčres et leur réimplantation sous-muqueuse.
Implications anesthésiques:
- L'injection de macroplastique est un geste peu douloureux, tant en peropératoire qu'en postopératoire, pratiquement assimilable ŕ la réalisation d'une simple cystoscopie. Une anesthésie générale classique, en ventilation spontanée ou assistée, sous masque laryngé le plus souvent, est tout ŕ fait appropriée.
En cas d’examen endoscopique des voies urinaires, il faut veiller ŕ utiliser un liquide réchauffé (pour éviter de provoquer une hypothermie qui s’installe d’autant plus rapidement que l’enfant est plus jeune) et d’utiliser du NaCl 0,9% afin d’éviter des accidents d’hyponatrémie par résorption ou extravasation. Il ne faut utiliser de l’H2O que dans les cas oů l’usage de courant électrique est nécessaire pour la chirurgie (incision d’urétérocčle).
- Les abords chirurgicaux ouverts sont des actes chirurgicaux invasifsL’incision est sous-ombilicale (de type Pfannenstiel). Ils sont réalisés sous anesthésie générale profonde, avec intubation trachéale ou pose d'un masque laryngé, et l'analgésie est idéalement assurée par un bloc périmédullaire, anesthésie caudale ou épidurale lombaire, avec anesthésiques locaux et adjuvants destinés ŕ prolonger l'analgésie pendant au moins 24h (clonidine ou morphine). La mise en place d'un cathéter de réinjection permet de poursuivre l’administration continue d’un mélange d’anesthésique local pendant 48 ŕ 72h. On peut également réaliser un bloc transverse de l’abdomen (TAP bloc) sous échoguidage
Un des problčmes de la chirurgie intravésicale est l’apparition de spasmes vésicaux postopératoires : leur suppression requiert un bloc sympathique étendu (racines T9 ŕ L2 mais aussi les afférences d’origine sacrée (S2-S4).Il semble que ces spasmes soient provoqués par la réactivation par l’inflammation locale de fibres C directement connectées au muscle détrusor Une étude a démontré que l’utilisation d’un cathéter caudal est plus efficace qu’un cathéter péridural lombaire pour prévenir ces spasmes. De plus, une position plus céphalique du cathéter entraînerait davantage de spasmes.
En l’absence de contre-indication ŕ l’administration d’un AINS (fonction rénale, hydratation, antibiotiques néphrotoxiques), l’administration systématique de kétorolac 0,5 mg/kg par voie IV 3 ŕ 4 fois par jour durant les deux premiers jours postopératoires permet habituellement de contrôler ces douleurs en diminuant la production intravésicale de prostaglandines. En cas de contre-indication aux AINS, on peut administrer un anticholinergique comme l’oxybutinine per os.
Références :
- Feld LG, Mattoo TK.
Urinary tract infections and vesicoureteral reflux in infants and children.
Pediatr Rev 2010; 31:451-63.
- Bell LE, Mattoo TK.
Update on childhood urinary tract infection and vesicoureteral reflux.
Semin Nephrol 2009; 29:349-59.
- Molitierno JA, Scherz HC, Kirsch AJ.
Endoscopic treatment of vesicoureteral reflux using dextranomer hyaluronic acid copolymer.
J Pediatr Urol 2008; 4:221-8.
- Szolnoki JM, Puskas F, Sweeney DM, Camporesi EM, Upadhyay J.
Hyponatremic seizures after suprapubic catheter placement in a 7-year-old child.
Pediatr Anesth 2006; 16:192-4.
- Park JM, Houck CS, Sethna NF, Sullivan LJ, Atala A, Borer JG, Cilento BG, Diamond DA, Peters CA, Retik AB, Bauer SB.
Ketorolac suppresses postoperative bladder spasms after pediatric ureteral reimplantation.
Anesth Analg 2000; 91: 11-5.
- Bryskin RB, Londergan B, Wheathley R, Heng R et al.
Transversus abdominis plane block versus caudal epidural for lower abdominal surgery in children.
Anesth Analg 2015; 121: 471-8
- Sommerfield D, Ramgolam A, Barker A, Bergesio R, von Ungern-Sternberg BS.
Epidural insertion height for ureteric reimplant surgery : does location matter ?
Pediatr Anesth 2016; 26: 951-9.
Mise-à-jour: octobre 2021