(Syndrome adénocutanéomuqueux)
Plus fréquent chez les enfants d’origine asiatique (incidence 240/100.000 enfants de moins de 5 ans au Japon vs 4-25/100.000 en Europe et aux USA) ou d’origine afro-caribéenne.Vascularite fébrile multisystémique d'étiologie inconnue : fičvre, conjonctivite, exanthčme polymorphe, vasculite, anévrysmes coronaires. C’est la cause la plus fréquente de pathologie cardiaque acquise chez l’enfant dans les pays développés. Cette vascularite touche principalement les enfants de moins de 5 ans (80%) (pic le nourrisson de 9-11 mois) et atteint les artčres de moyen calibre (coronaires, mésentériques, iliaques). La cause en est sans doute un agent infectieux encore inconnu qui entraîne une réaction immunitaire particuličre (augmentation des lymphocytes B circulants) chez des individus génétiquement prédisposés. En l’absence de traitement, des anévrysmes des artčres coronaires se développent dans 18-23 % des cas (et dans moins de 5 % en cas de traitement précoce) et il y a un risque de décčs par myocardite, dysfonction du VG ou infarctus du myocarde. Il existe d’autres complications et modes de présentation de la maladie : méningite aseptique, pneumonie avec épanchement pleural, cholécystite, pancréatite, myosite, péricardite.
En l’absence de test diagnostique, le diagnostic est clinique :
Critčres diagnostiques de la maladie de Kawasaki
|
1 |
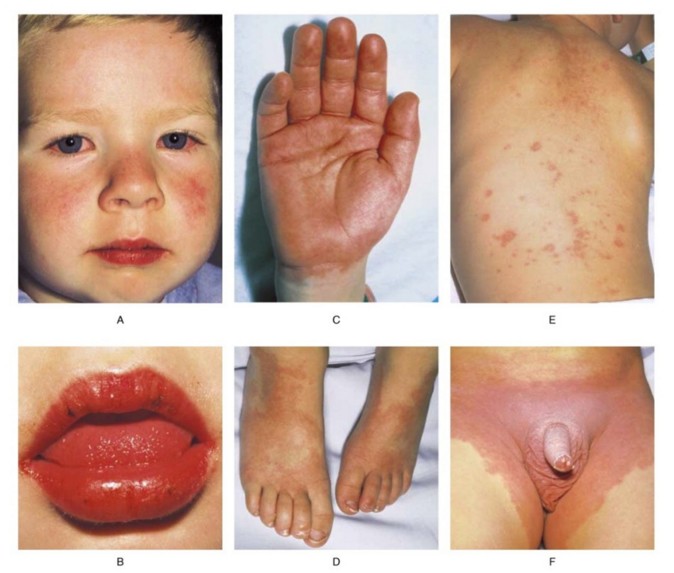
Injection conjonctivale bilatérale non-exsudative (a) |
|
2 |
Adénopathie cervicale : au moins 1 ganglion de diamčtre >1,5 cm |
|
3 |
Rash maculopapuleux diffus, morbilliforme ou scarlatiniforme au niveau du tronc et des membres, localisation périnéale typique(e, f) |
|
4 |
Atteinte oropharyngée :chéilite, stomatite, langue framboisée (b) |
|
5 |
Atteinte des pieds et des mains : oedčme, induration, desquamation (c, d) |
On distingue :
Kawasaki classique ou typique si fičvre depuis ≥ 5 jours et ≥ 4 des 5 critčres, ou
si fičvre depuis ≥ 5 jours et ≥ 4 des 5 critčres et anévrismes coronaires
Kawasaki incomplet ou atypique si fičvre depuis ≥ 5 jours et ≥ 2 des 5 critčres.
Les patients souffrant d’une forme incomplčte ont un risque majoré de développer des anévrismes coronaires car le diagnostic est retardé voire manqué.
Une étude épidémiologique récente a permis d’identifier 4 sous-groupes en fonction du mode principal de présentation et de l’âge :
|
Signe principal |
Atteinte hépatique |
Neutrophiles immatures
|
Adénopathies cervicales |
Jeune âge |
|
âge |
+âgé |
intermédiaire |
intermédiaire |
+ jeune |
|
Incidence adénopathies |
intermédiaire |
basse |
élevée |
basse |
|
|
SGPT, ăGT et bilirubine totale élevés, hémoglobine élevée |
Neutrophiles immatures ++ mais globules blancs et plaquettes bas |
Globules blancs et plaquettes élevés ; CRP trčs élevée ; hémoglobine basse |
Globules blancs (surtout lymphocytes) et plaquettes trčs élevés ; CRP peu élevée |
|
Risque
|
|
intermédiaire |
intermédiaire |
élevé |
|
Résistance aux gammaglobulines |
élevée |
intermédiaire |
intermédiaire |
basse |
|
Incidence
|
basse |
élevée |
intermédiaire |
basse |
Critčres échographiques de l’atteinte coronarienne :
* Z-score de l’artčre interventriculaire antérieure (IVA) ou de l’artčre coronaire droite (ACD) ≥ 2,5
* Présence d’un anévrisme coronarien
* ≥ 3 des critčres suivants :
- diminution de la fonction systolique ventriculaire gauche
- insuffisance mitrale
- épanchement péricardique
- et/ou Z-score de l’IVA ou de l’ACD de 2‑2,5
Classification de l’atteinte coronaire en fonction du Z score
Degré d’atteinte coronarienne Diamčtre coronarien en Z-score ± dimension absolue
1. Pas d’atteinte Toujours < 2
2. Dilatation seule 2 ŕ < 2,5 ; ou si initialement < 2, diminution
du Z-score de ≥ 1 durant le suivi
3. Anévrisme de petite taille ≥ 2,5 a < 5
4. Anévrisme de taille moyenne ≥ 5 a < 10 et dimension absolue < 8 mm
5. Anévrisme de grande taille
ou géant ≥ 10 ou dimension absolue ≥ 8 mm
Durant la forme aiguë de la maladie, l’enfant peut présenter deux formes plus sévčres :
- soit une forme de choc cardiogénique (KDSS pour Kawasaki Disease Shock Syndrome) : hypotension artérielle avec ou sans vasoconstriction, rebelle au traitement et accompagnée de signes échocardiographiques (dysfonction du VG, régurgitation mitrale, épanchement péricardique) et biologiques de myocardite (troponine) ou d’insuffisance cardiaque (proBNP).
- soit une forme d’activation macrophagique (MAS pour Macrophage Activation Syndrome), une forme d’hémophagocytose lymphohistiocytaire d’origine virale avec orage cytokinique (voir ce terme)
Un syndrome proche de la maladie de Kawasaki (ou PMIS, acronyme en anglais de Pediatric Multisystem Inflammatory Syndrome) (voir ce terme) a été observé durant la pandémie du COVID-19 : il touchait des enfants en général âgés de plus de 5 ans dans un tableau de fičvre de plusieurs jours avec diarrhées et douleurs abdominales, évoluant vers un état hyperinflammatoire (orage cytokinique) intermédiaire entre le syndrome de Kawasaki typique et le choc toxinique. La plupart de ces cas avaient été infectés par le COVID 19 et tous ont répondu favorablement ŕ l’administration d’immunoglobulines et de corticostéroďdes.
L’évolution spontanée de la forme classique maladie se déroule en 3 phases :
L’évolution spontanée de la maladie se déroule en 3 phases :
- phase aiguë (du 1er au 7-14ème jour) : fièvre rebelle aux antibiotiques. L’atteinte cardiaque peut se présenter comme un BAV partiel, des troubles de la repolarisation (onde T aplatie), une hypokinésie du VG et du VD, un épanchement péricardique, une dilatation des coronaires…
- phase subaiguë (du 10ème au 25ème jour) : la fièvre a souvent disparu et les extrémités desquament. Des anévrysmes artériels, notamment coronariens, sont présents dans 20% des cas. Il existe une thrombocytose importante avec risque de thrombose et d’ischémie. Le diagnostic n’est pas évident à poser durant ces deux périodes car les signes de l’affection ne sont pas tous toujours présents en même temps ; de plus, la présentation peut être atypique : méningite ou arthrite aseptique par exemple.
- phase de convalescence (6 à 8 semaines après le début) : en l’absence de traitement, l'évolution propre des lésions vasculaires se fait vers la thrombose avec infarctus myocardique, rupture de piliers, angor. L’angor est souvent silencieux (ses manifestations cliniques sont difficiles à interpréter chez le petit enfant) et l’ECG peu spécifique.
L’algorithme de prise en charge recommandé par l’AHA est
.jpg)
Le traitement recommandé ŕ l’heure actuelle repose sur un diagnostic précoce et un suivi spécialisé :
- phase aiguë :
- aspirine 80-100 mg/kg en 4 doses jusqu’ŕ la défervescence puis 2-5 mg/kg/jour pendant au moins 6 semaines
- gammaglobulines humaines : 2g/kg IV en dose unique si CRP > 30 mg/L
- surveillance ECG et échographique
- aprčs défervescence (48 h), répéter une échocardiographie ŕ 2 et 6 semaines et selon le résultat :
- en l'absence d’anévrysmes coronaires : aspirine ŕ faible dose jusqu’ŕ 6 semaines
- en présence d'anévrysmes coronaires de diamčtre < 6 mm, sans sténoses : répéter les échographies tous les 6 mois et poursuivre l’aspirine jusqu’ŕ la disparition des anévrysmes
- en présence d'anévrysmes coronaires de diamčtre > 6 mm, et/ou sténoses : poursuivre l’aspirine et envisager un traitement anticoagulant ŕ base d’antivitamines K ; continuer l’aspirine et proposer une prophylaxie de l’athéromatose ; répéter les échographies tous les 6 mois (éventuellement coronarographie et épreuve d’effort)
- en l’absence de défervescence aprčs 48h ou en cas de rechute dans les 2 semaines (dans 20% des cas environ) : répéter une dose de gammaglobulines et ajouter une corticothérapie (méthylprednisolone 30 mg/kg/j). L’infliximab (5 mg/kg en 1 dose IV) est utilisé en cas de non-réponse ŕ la corticothérapie ou de forme trčs sévčre.
Les enfants porteurs d‘anévrismes coronaires géants (z-score ≥ 10 ou diamčtre ≥ 8 mm) présentent un risque élevé d’événements cardiovasculaires graves dont des infarctus myocardiques de type STEMI ou non-STEMI. La prise en charge en est similaire ŕ celle chez l’adulte: coronarographie en urgence le plus souvent avec fibrinolyse.
En bref:
* STEMI (ischémie sévčre et nécrose myocardique)
- accčs au cathétérisme cardiaque < 90 min aprčs le premier contact médical
- nourrisson : clopidogrel p os 0,2 mg/kg si nourrisson, 1 mg/kg si enfant ; prasugrel 60 mg si adolescent
- héparine IV dčs que l’accčs veineux est obtenu : 75 UI/kg suivi de 20 UI/kg/h
- si gros thrombus : aspiration non recommandée mais envisager un antagoniste des récepteurs plaquettaires IIb/IIIa : eptifibitide 180µg/kg puis 2 µg/kg/h pendant 12h
- accčs au cathétérisme cardiaque > 90 min aprčs le premier contact médical
- en attendant le transfert en salle de cathétérisme : activateur du plasminogčne tissulaire (tPA) : 0,03 ŕ 0,1 mg/kg/h pendant 6-12h, max 2 mg/h ; attention le taux de fibrinogčne doit ętre > 150 mg/dl sinon il faut administrer 10-20 ml/kg de PFC
- débuter héparine IV 10U/kg/h sur une voie veineuse différente du tPA, et poursuivre pendant 6h aprčs l’arręt du tPA.
- Coronarographie dčs que possible
- pas d’accčs au cathétérisme cardiaque
- débuter le traitement par activateur du plasminogčne tissulaire (tPA) : 0,03 ŕ 0,1 mg/kg/h pendant 6-12h, max 2 mg/h ; attention le taux de fibrinogčne doit ętre > 150 mg/dl sinon il faut administrer 10-20 ml/kg de PFC
- débuter héparine IV 10U/kg/h sur une voie veineuse différente du tPA ;
- vérifier le taux d’antithrombine III et en administrer pour obtenir un taux sanguin de v80 ŕ 120%
- ŕ l’arręt du tPA, adapter la dose d’héparine pour obtenir un temps de coagulation activée de 200-250 sec
- pour inhiber l’aggrégation plaquettaire : envisager un antagoniste des récepteurs plaquettaires IIb/IIIa : eptifibitide 180µg/kg puis 2 µg/kg/h pendant 12h (données chez l’adulte)
- en cas de douleurs thoraciques : administrer un dérivé nitré par voie sublinguale ou IV ; attention au risque d’hypotension
* non-STEMI (apport insuffisant d’O2 au myocarde sans nécrose) : anomalies ECG et augmentation des troponines :
1) débuter héparine IV : 75 IU/kg puis 20U/kg/h en fonction du taux d’antiXa
2) débuter ou poursuivre l’aspirine et débuter le clopidogrel p os : 2-3 mg/kg en dose
de charge suivi de 1 mg/kg/j (max 75 mg)
3) réaliser une imagerie des coronaires (CT ou coronarographie
Implications anesthésiques:
Si coronaropathie, vérifier la fonction myocardique par une échocardiographie préopératoire. ECG 5 dérivations. Y penser en présence d’un enfant de moins de 5 ans fébrile avec une éruption et/ou des ganglions ou en cas de problčme cardiaque périopératoire imprévisible (situation ŕ risque : laparotomie blanche pour suspicion d’appendicite).
Références :
- Morrison JE, Anderson M, Chan KC, Pietra B, Zuk J, Gnadinger P.
A 15-year review of children with Kawasaki’s syndrome having general anesthesia or sedation.
Pediatr Anesth 2005; 15: 1053-8.
- Bressieux-Degueldre S, Schaffner D, Hofer M, Sekarski N, Vanoni F.
Maladie de Kawasaki : mise ŕ jour.
Revue Médicale Suisse 2018 ; 14 : 384-9
- McCrindle BW, Rowley AH, Newburger JW, et al.
Diagnosis, treatment, and long-term management of Kawasaki disease: a scientific statement for health professionals from the American Heart Association.
Circulation 2017; 135: e927–99.
- Riphagen S, Gomez J, Gonzalez-Martinez C, Wilkinson N, Theocharis P.
Hyperinflammatory shock in children during COVID-19 pandemic.
The Lancet doi.org/10.1016/S0140-6736(20)31094-1 (May 6, 2020)
- Verdoni L, Mazza A, Gervasoni A, Martelli L, Ruggeri M, Ciuffreda M, Bonanomi E, D’Antiga L.
An outbreak of severe Kawasaki-like disease at the Italian epicentre of the SARS-CoV-2 epidemic: an observational cohort study.
The Lancet doi.org/10.1016/S0140-6736(20)31103-X (May 13, 2020)
- Burns JC, El-Said H, Tremoulet AH, Friedman K, Gordon JB, Newburger JW.
Management of myocardial infarction in children with giant coronary artery aneurysms after Kawasaki disease.
J Pediatr 2020 ; 120 : 230-4.
- Wang H, Shimizu C, Bainto E, Hamilton S, Jackson HR, Estrada-Rivadeneyra D, Kaforou M et al.
Subgroups of children with Kawasaki disease: a data-driven cluster analysis.
Lancet Child Adolesc Health 2023; 7: 697–707.
Mise-à-jour septembre 2023